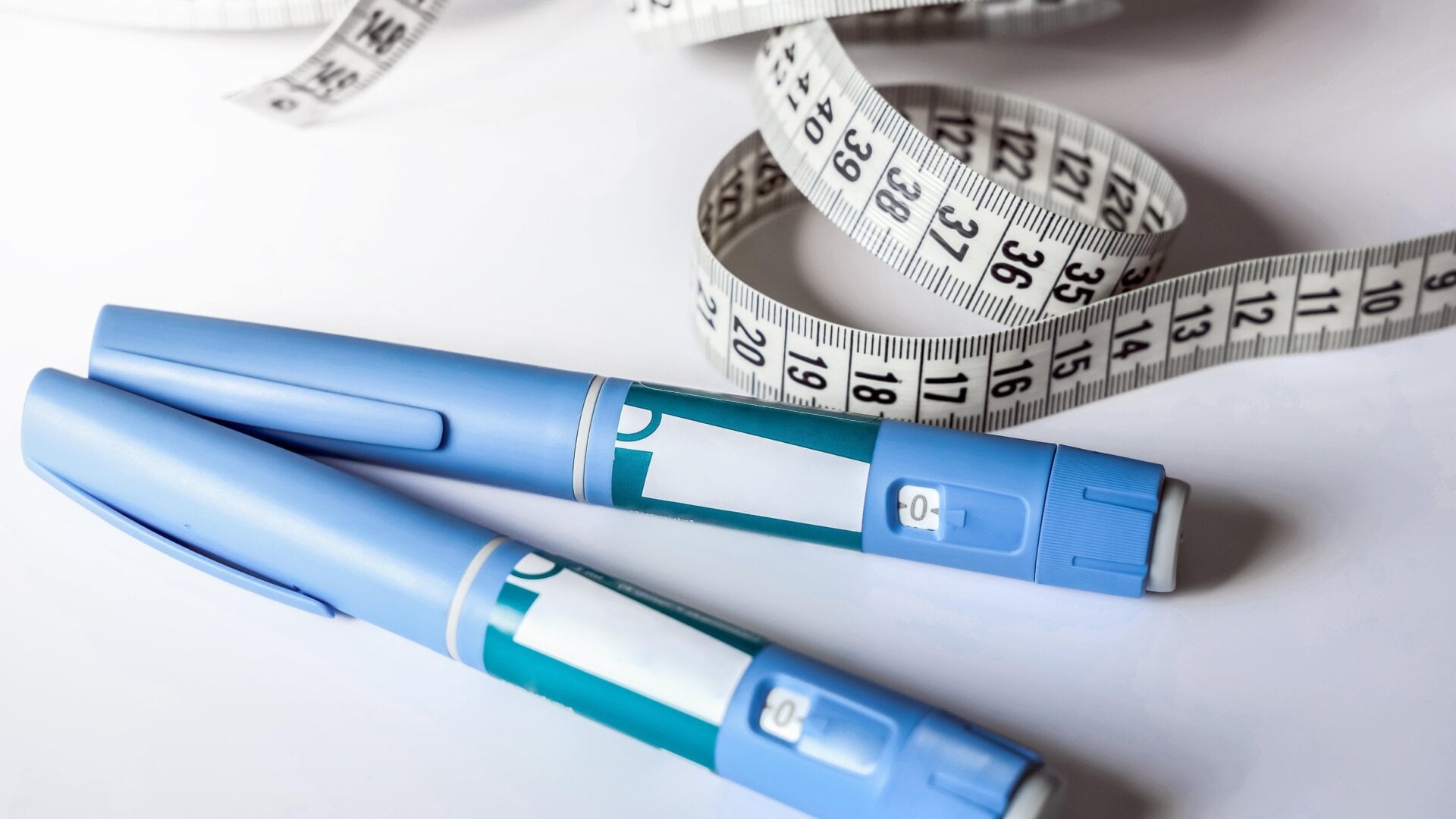
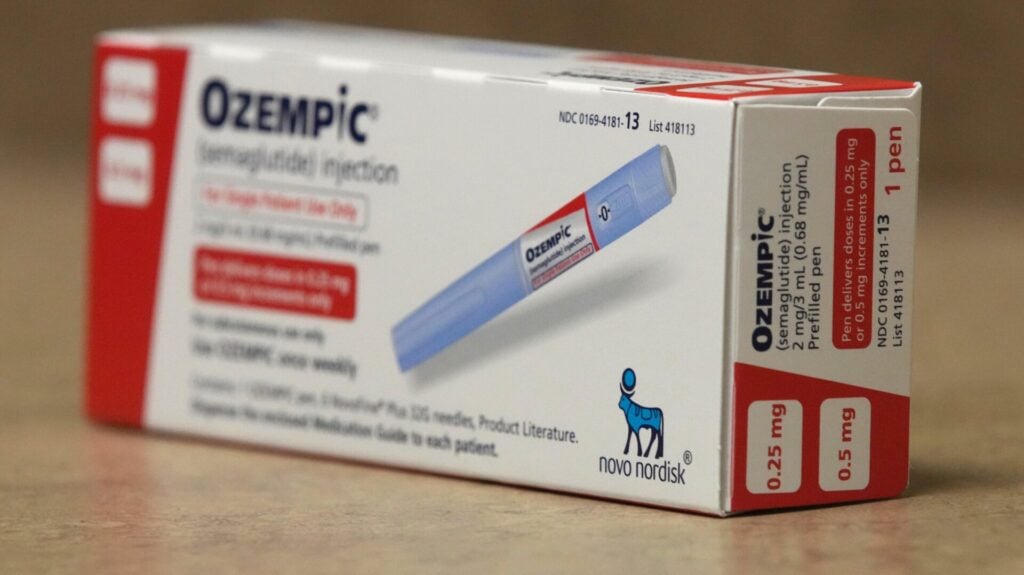
Les résultats d’une enquête de neuf mois menée par les organismes de réglementation de la santé dans l’Union européenne devraient être réconfortants pour toute personne prenant Ozempic et d’autres médicaments similaires. pour traiter leur diabète de type 2 et/ou leur obésité. Les responsables de l’UE ont annoncé vendredi qu’ils n’avaient pas réussi à trouver la preuve d’un lien de causalité entre les BPL et 1 drogues et un risque accru de suicide ou d’idées suicides.
L’été dernier, les régulateurs de la santé en Islande, au Royaume-Uni et dans l’UE ont révélé qu’ils avaient reçu des rapports de cas liant l’utilisation du GLP-1. médicaments contre les idées suicidaires. Les médicaments mentionnés dans ces rapports étaient le liraglutide et le sémaglutide, ce dernier étant le premier d’une série de médicaments. nouvelle génération, beaucoup plus efficace de médicaments anti-obésité (Ozempic est la marque de sémaglutide approuvée pour le diabète de type 2, tandis que Wegovy est approuvée pour l’obésité).
En réponse à ces rapports, l’Agence européenne des médicaments (la version européenne de la Food and Drug Administration) a annoncé qu’elle nommerait des membres. de son comité d’évaluation des risques de pharmacovigilance pour effectuer un examen de ces médicaments et d’autres médicaments GLP-1. Les constatations de l’examen ont été détaillées lors de la dernière réunion du PRAC cette semaine, et ils sont très rassurants.
« Le PRAC a conclu que les preuves disponibles ne soutiennent pas une association causale entre les agonistes des récepteurs du peptide-1 de type glucagon (GLP-1) – dulaglutide, exénatide, liraglutide, lixisénatide et semaglutide – et des pensées et actions suicidaires et d’automutilation », a annoncé l’EMA dans un communiqué. libéré Vendredi.
Pour parvenir à leurs conclusions, les auteurs de la revue ont analysé des rapports de cas, des données collectées auprès des fabricants de médicaments et les résultats d’une enquête. étude récente de dossiers de santé électroniques (qui n’a pas trouvé un lien entre le suicide et l’utilisation du GLP-1). L’EMA a également mené une enquête séparée une analyse des dossiers de santé qui se concentrait spécifiquement sur les personnes prenant des GLP-1 pour leur diabète de type 2 et qui, de la même manière, n’a trouvé aucun lien.
L’enquête de l’EMA est la deuxième enquête récente menée par les organismes de réglementation de la santé pour exclure les médicaments GLP-1 des causes de suicide. En janvier, la FDA a signalé que son évaluation préliminaire n’avait trouvé aucune preuve d’un risque de suicide. Et certaines recherches récentes ont même suggéré que les médicaments GLP-1 pourraient avoir des avantages en matière de santé mentale, comme un papier publié plus tôt en février, cette étude a révélé que l’utilisation du GLP-1 était liée à des taux plus faibles d’anxiété et de dépression.
Bien sûr, les GLP-1 ont leurs inconvénients. Ils provoquent généralement des nausées et d’autres symptômes gastro-intestinaux, par exemple. Ils ont également été liés à d’autres probablescomplications rares mais graves comme la gastroparésie. Et comme pour tout médicament, tous ceux qui pourraient bénéficier de leur prise ne répondront pas ou ne pourront pas tolérer le effets secondaires.
La FDA a déclaré en janvier qu’elle était encore en train de finaliser les résultats de son enquête sur le lien entre l’utilisation du GLP-1 et le suicide. L’EMA a déclaré vendredi que les fabricants de médicaments GLP-1 continueront à surveiller leurs données pour détecter ces complications et d’autres complications potentielles et signaleront tout nouveau problème. constatations dans le fait des pratiques de sécurité standard après approbation.